FAVEA провела семинар «Валидация компьютерных систем на фармацевтических производствах»
4 июля 2017 года в Москве прошел организованный FAVEA Group семинар на тему «Валидация компьютерных систем на фармацевтических производствах». В семинаре приняли участие более 60 специалистов из России и стран ближнего и дальнего зарубежья не только различных фармацевтических производств, но и компаний, осуществляющих поставку и монтаж фармацевтического оборудования, занимающихся разработкой и внедрением IT-систем на предприятиях и из других смежных и вспомогательных отраслей.
Лектором семинара являлся Директор по качеству FAVEA Group Зденек Павелек, имеющий многолетний опыт работы в фармацевтической отрасли.
Валидация компьютерных систем (КС) – одна из наиболее актуальных задач любого современного фармацевтического производства. При этом задача сложная и, для многих производств, новая. Вот почему семинар был начат с лекции, основанной на Приложении 11 Правил GMP «Компьютеризированные системы», в ходе которой были освящены основные принципы и подходы к использованию компьютерных систем в ходе всего их жизненного цикла с подробным рассмотрением фаз проектирования и эксплуатации КС: анализ рисков, составление описаний критических систем и спецификаций, а также требований к контролю и сохранению данных, их прослеживаемости и т.д.
Вторая лекция была посвящена руководству ЕС GMP и надлежащей практике автоматизированного производства (GAMP). Данная презентация, помимо разъяснений в целом, что представляет из себя надлежащая практика автоматизированного производства, охватывала вопросы структуры руководства и общей концепции GAMP, методов и фаз жизненного цикла с детализацией каждой фазы, а также другие вопросы применения на практике вышеуказанных руководств при валидации КС.
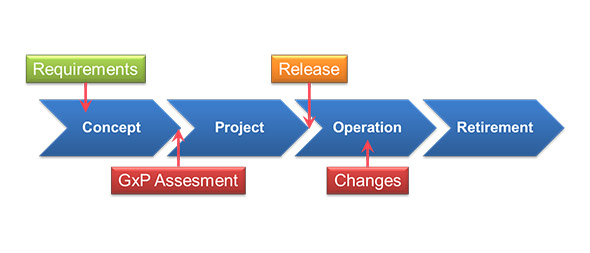
Подробно каждая стадия валидации КС на различных этапах жизненного цикла была рассмотрена Зденеком в презентации «Жизненный цикл и валидация компьютерных систем управления». Лекция включала в себя материалы по планированию проектной и валидационной деятельности, особенностям каждой из них на разных стадиях, а также рассмотрение ключевых моменты валидационных работ применительно к КС.
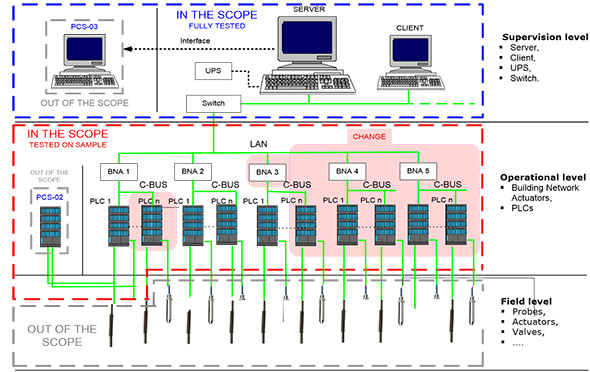
Наибольший интерес вызвала практическая часть семинара – разбор примера полной валидации системы управления воздухоподготовкой (HVAC), начиная от составления плана валидации на основании оценки рисков и завершая примером оформления отчета. Также были рассмотрены аспекты составления технических требований пользователя (URS), включая общие требования, требования к технологическому процессу, к автоматизации и безопасности и, безусловно, к документации. Кроме того, для каждой из стадий валидации (IQ, OQ и PQ) приводились примеры выполняемых тестов с интерпретацией полученных результатов.
Завершался семинар лекцией по контролю изменений компьютерных систем: Зденек рассказал о видах изменений, их градации и идентификации, методе оценки, а также о выполнении контроля.
По окончании семинара участники получили именные сертификаты.
Некоторые отзывы участников о семинаре: «Очень полезный семинар для общего понимания принципов и подходов квалификации автоматизированных систем управления на фармацевтических производствах». «Интересный семинар, дающий четкое представление как правильно организовать комплекс валидационных мероприятий для соответствия стандартам GMP». «Очень высокопрофессиональный уровень преподавателя и доступность изложения материала. Спасибо!» «Заявленные темы раскрыты, ожидания удовлетворены в полной мере!»